Mini-Gehirne zeigen, warum Alzheimer-Medikamente oft unterschiedlich wirken
Kleine Hirnmodelle aus dem Labor liefern neue Einblicke in Alzheimer. Sie zeigen, warum Behandlungen nicht bei allen Betroffenen gleich anschlagen.
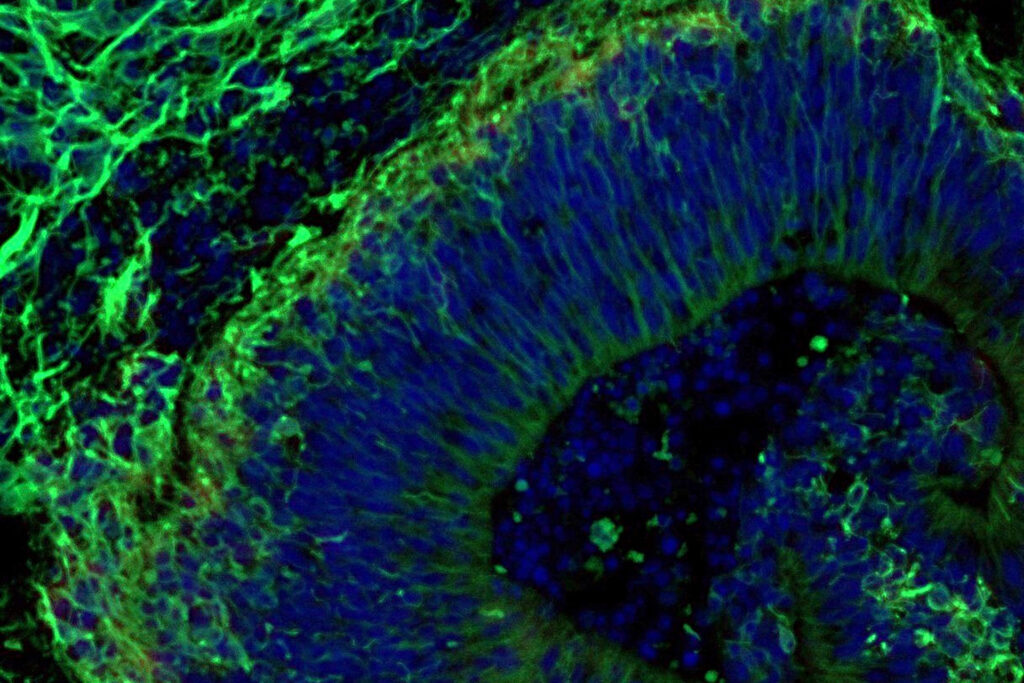
Das Bild zeigt ein im Labor gezüchtetes Mini-Gehirn, das Hinweise darauf liefert, wie sich Alzheimer früher erkennen lässt. Grün markierte Nervenzellen und blau dargestellte Zellkerne machen die Struktur des Organoids sichtbar (Maßstab: 50 Mikrometer). © Machairaki lab
Bei Alzheimer kommen oft Medikamente zum Einsatz, die Begleiterscheinungen wie Angst, Depression oder Unruhe lindern sollen. Doch manche Patienten sprechen gut darauf an, andere kaum. Das macht die Behandlung so schwierig. Sogenannte Organoide könnten bei Alzheimer nun helfen, diese Unterschiede besser zu verstehen. Organoide sind kleine Gewebestrukturen, die aus menschlichen Zellen im Labor entstehen. Sie bilden wichtige Funktionen des Gehirns nach. Forschende können damit Krankheiten untersuchen und Therapien vorab testen.
Ein Team von Johns Hopkins Medicine hat solche Modelle genauer analysiert. Grundlage der Untersuchung waren Zellen von 30 Personen, darunter 24 mit Alzheimer. Daraus entstanden kleine, erbsengroße Hirnmodelle. Sie ahmen vor allem das Hinterhirn nach, das unter anderem Atmung, Schlaf und Herzfrequenz steuert.
Da diese Modelle direkt von Patienten stammen, tragen sie deren individuelle biologischen Merkmale in sich. Im nächsten Schritt testete das Team ein bekanntes Medikament: Escitalopram. Es wird häufig bei psychischen Begleitsymptomen eingesetzt. Die Reaktionen im Labor fielen jedoch sehr unterschiedlich aus.
Organoide machen Unterschiede bei Alzheimer erstmals sichtbar
Ein Teil der Organoide reagierte deutlich. Bestimmte Eiweiße, die für die Kommunikation zwischen Nervenzellen wichtig sind, nahmen zu. In anderen Modellen zeigte sich kaum eine Veränderung.
Studienleiterin Vasiliki Machairaki von der Johns Hopkins University School of Medicine erkärt: „Unsere Studie legt nahe, dass große, patientenbasierte Hirnorganoide und die von ihnen freigesetzten Vesikel helfen können, Alzheimer einzuordnen, Krankheitsmechanismen zu untersuchen und zu verstehen, wie verschiedene Patientengruppen auf Behandlungen reagieren.“
Erste Hinweise auf Patienten ohne Wirkung
Die Unterschiede lassen sich bis auf die Ebene einzelner Eiweiße zurückverfolgen. In den Modellen veränderten sich bei einigen Proben zahlreiche Moleküle. Andere reagierten kaum.
Das deutet auf sogenannte Nicht-Responder hin. Gemeint sind Patienten, bei denen ein Medikament keine messbare Wirkung zeigt. Diese Gruppe lässt sich bisher kaum erkennen. Die Laborergebnisse zeigen erstmals:
- Manche Patienten reagieren klar auf bestimmte Wirkstoffe
- Andere zeigen kaum biologische Veränderungen
- Unterschiede lassen sich bereits im Zellmodell sichtbar machen
Zellpartikel liefern zusätzliche Informationen aus dem Gehirn
Neben den Mini-Gehirnen untersuchte das Team auch sogenannte extrazelluläre Vesikel. Das sind winzige Partikel, die Zellen nach außen abgeben. Sie transportieren Informationen über den Zustand der Zellen. Diese Vesikel enthalten Eiweiße, die für zentrale Hirnfunktionen wichtig sind. Dazu gehören Prozesse wie Gedächtnis, Signalübertragung und die Freisetzung von Botenstoffen.
Bei Alzheimer-Proben zeigten sich klare Unterschiede. Einige wichtige Proteine lagen in geringerer Menge vor. Dazu zählen etwa RAB3A, NSF und ATCAY. Diese Moleküle spielen eine wichtige Rolle bei der Kommunikation zwischen Nervenzellen. Nach der Behandlung mit Escitalopram stiegen einige dieser Werte wieder an – allerdings nur in bestimmten Proben.
Neue Chance für Diagnose und Krankheitsverlauf
Die Vesikel könnten künftig eine wichtige Rolle spielen. Sie lassen sich möglicherweise im Blut nachweisen. Dadurch entsteht eine neue Perspektive für die Diagnostik. Die Forschenden sehen darin eine mögliche „flüssige Biopsie“. Gemeint ist eine Untersuchung, die ohne Eingriff ins Gehirn auskommt. Sie könnte helfen, Alzheimer früher zu erkennen und den Verlauf besser einzuschätzen. Machairaki erklärt:
Unser Modell könnte künftig helfen, Patientengruppen zu identifizieren, die eher auf bestimmte Medikamente ansprechen, und so gezieltere Behandlungen ermöglichen.
Warum Alzheimer so unterschiedlich verläuft
Ein Grund für die unterschiedlichen Reaktionen liegt in der Natur der Krankheit. Alzheimer ist keine einheitliche Erkrankung. Mehr als 90 genetische Faktoren stehen mit dem Risiko in Verbindung.
Diese Vielfalt zeigt sich auch in den Laborergebnissen. Jeder Krankheitsverlauf weist eigene biologische Muster auf. Diese Unterschiede machen die Behandlung so schwierig. Die Organoide bilden diese Vielfalt erstmals direkt ab. Sie zeigen, wie unterschiedlich Prozesse im Gehirn verlaufen können.
Die Ergebnisse stammen aus Laborversuchen. Die Modelle bilden nicht das komplette Gehirn ab. Wichtige Bestandteile wie Blutgefäße fehlen noch. Trotzdem liefern sie wichtige Hinweise. Sie zeigen, wie stark die Wirkung von Medikamenten vom individuellen biologischen Profil abhängt.
Kurz zusammengefasst:
- Organoide aus Patientenzellen bilden Alzheimer im Labor nach und zeigen, dass Medikamente je nach Person sehr unterschiedlich wirken können.
- In den Modellen reagieren manche Proben klar auf Wirkstoffe, andere kaum, was auf bisher schwer erkennbare Nicht-Responder hinweist.
- Zusätzlich liefern Zellpartikel messbare Hinweise auf frühe Krankheitsprozesse und könnten künftig Diagnose und Therapie gezielter machen.
Übrigens: Während Organoide bei Alzheimer individuelle Unterschiede sichtbar machen, zeigen neue Daten, dass das Immunsystem im Gehirn oft nach festen Mustern arbeitet – selbst bei ganz verschiedenen Krankheiten. Wie diese Programme funktionieren und warum ihr Ort im Gehirn entscheidend ist, mehr dazu in unserem Artikel.
Bild: © Machairaki lab











