Ein unscheinbares Protein programmiert Bakterien auf Angriff
Ein Protein steuert, ob Bakterien gefährlich werden. Blockiert man diesen Schalter, könnten Infektionen ohne Antibiotika abgeschwächt werden.
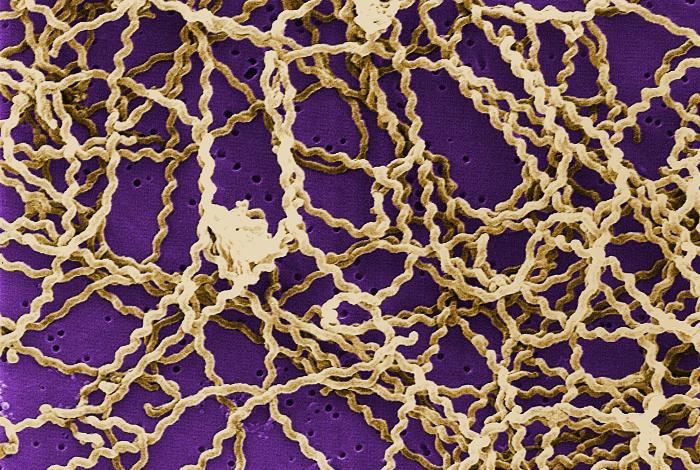
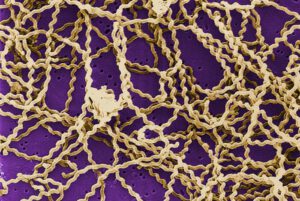
Das Bakterium Leptospira ist genau so harmlos, wie es aussieht. Bis ein Protein im Inneren auf Angriff schaltet. © Wikimedia
Bakterielle Infektionen können harmlos bleiben, doch manche nehmen einen gefährlichen Verlauf. Beispielsweise bei der Leptospirose, hier reicht das Verlaufsspektrum von asymptomatisch bis hin zu tödlich. Ob eine Infektion mit dem Bakterium Leptospira leicht oder schwer verläuft, entscheidet ein unscheinbares Protein im Inneren des Bakteriums. Denn diese Bakterien sind nicht dauerhaft gefährlich. Sie aktivieren ihre Angriffsfähigkeit erst im richtigen Moment. Eben diesen Mechanismus hat ein Forschungsteam nun entschlüsselt. Die Ergebnisse stammen aus einer Studie der Universität Basel, veröffentlicht im Fachjournal Nature Communications.
Das Protein funktioniert dabei wie ein Schalter und entscheidet, wann ein Erreger im Körper aktiv wird. Dieser Baustein steuert das Angriffspotenzial des Bakteriums Leptospira. Blockiert man diesen Schalter, könnten Infektionen auch ohne Antibiotika abgeschwächt werden.
Krankheitserreger werden erst im Körper gefährlich
Mit Leptospirose infizieren sich Menschen meist über verunreinigtes Wasser oder Erde, die Träger der Leptospira-Bakterien sind Nager oder infizierte Nutztiere. Weltweit erkranken jedes Jahr rund eine Million Menschen schwer. Etwa 60.000 sterben daran. Ohne schnelle Behandlung droht Organversagen.
Besonders in Regionen mit wenig medizinischer Versorgung ist die Krankheit ein großes Problem. Auch in Europa treten immer wieder Fälle auf, vor allem bei Landwirten, Tierärzten, Laborpersonal oder Kanalarbeitern.
Ein Protein hält den Erreger vorerst in Schach
Der Erreger verhält sich zunächst unauffällig. Erst im Körper aktiviert er gezielt seine krankmachenden Eigenschaften. Im Zentrum steht das Protein LvrB. Es steuert, ob das Bakterium gefährlich wird. Im Ruhezustand bleibt LvrB blockiert.
„Im Aus-Zustand ist LvrB in einer symmetrischen und damit inaktiven Form fixiert, in der es keine Virulenzfaktoren aktivieren kann“, erklärt Erstautor Elia Agustoni. In diesem Zustand produziert der Erreger keine krankmachenden Faktoren. Das spart Energie und verhindert unnötige Aktivität außerhalb eines Wirts.
Ein Signal kippt die Struktur und startet den Angriff
Sobald das Bakterium in den Körper gelangt, ändern sich die Bedingungen. Signale vom Wirt lösen zunächst eine chemische Reaktion aus. „LvrB verändert seine Form, die Symmetrie wird aufgebrochen, wodurch das Protein quasi aktiviert wird“, sagt Agustoni. Die zuvor blockierten Bereiche werden beweglich. Das Protein kann sich selbst aktivieren und gibt Signale weiter.
Nach der Aktivierung arbeitet LvrB mit einem Partnerprotein namens LvrC zusammen. Dieses wirkt als sogenannter Anti-σ-Faktor und greift direkt in die Gensteuerung ein. Innerhalb kurzer Zeit werden hunderte Gene umprogrammiert. Sie steuern die Angriffsfähigkeit des Erregers:
- Der Erreger kann sich im Körper vermehren
- Er kann Gewebe befallen
- Er kann das Immunsystem umgehen
So passt sich das Bakterium gezielt an seine Umgebung an und breitet sich aus.
Neuer Therapieansatz setzt direkt am Schalter an
Die Erkenntnisse aus der Baseler Studie eröffnen neue Wege in der Medizin. Statt Bakterien abzutöten, lässt sich ihr Gefahrenpotenzial blockieren. Bleibt LvrB inaktiv, kann der Erreger keine Krankheit auslösen. Studienleiter Sebastian Hiller sagt: „Gelänge es, LvrB dauerhaft auszuschalten, könnte man verhindern, dass der Erreger im Körper auf ‚virulent‘, also auf ‚gefährlich‘ umschaltet.“
Ein solcher Ansatz bietet mehrere Vorteile:
- Der Erreger bleibt zwar vorhanden, richtet aber keinen Schaden an
- Der Selektionsdruck sinkt, Resistenzen entstehen langsamer
- Therapien könnten gezielter wirken
Fachleute sehen in der Blockade des Proteins eine mögliche Alternative zu klassischen Antibiotika.
Mechanismus könnte viele Krankheitserreger betreffen
Das Protein LvrB gehört zu einer größeren Gruppe von sogenannten Histidin-Kinasen. Diese kommen in vielen Bakterien vor. Der jetzt entschlüsselte Mechanismus liefert ein Modell für ähnliche Systeme.
„Wir verstehen nun auf atomarer Ebene, wie dieser molekulare Schalter funktioniert“, sagt Hiller. „Und noch wichtiger, wir haben einen generellen Aktivierungsmechanismus entdeckt, der eine Vielzahl weiterer bakterieller Proteine betrifft.“ Damit wächst die Chance, neue Wirkstoffe zu entwickeln, die gezielt an solchen Schaltern ansetzen.
Kurz zusammengefasst:
- Krankheitserreger werden nicht dauerhaft gefährlich, sondern aktivieren ihre Angriffsfähigkeit erst im Körper über einen präzisen molekularen Schalter wie das Protein LvrB.
- Dieser Schalter verändert seine Struktur durch Signale des Wirts, aktiviert dadurch hunderte Gene und ermöglicht dem Erreger, sich anzupassen, sich zu vermehren und das Immunsystem zu umgehen.
- Neue Therapien könnten ansetzen, indem sie den Schalter blockieren und Krankheitserreger unschädlich machen.
Übrigens: Ähnlich wie Bakterien schalten auch Pilze ihre Gefährlichkeit durch Aktivierung bestimmter Mechanismen frei – vor allem bei Wärme und im menschlichen Körper. Was dahinter steckt und warum daraus neue Krankheitserreger entstehen können, mehr dazu in unserem Artikel.
Bild: © CDC/ Rob Weyant via Wikimedia unter Public Domain