Neue Krebstherapie drängt Tumore zurück – ganz ohne Chemotherapie
Eine neue CAR-T-Zelltherapie erzielte bei Blutkrebs komplette Remissionen – ohne vorbereitende Chemotherapie.
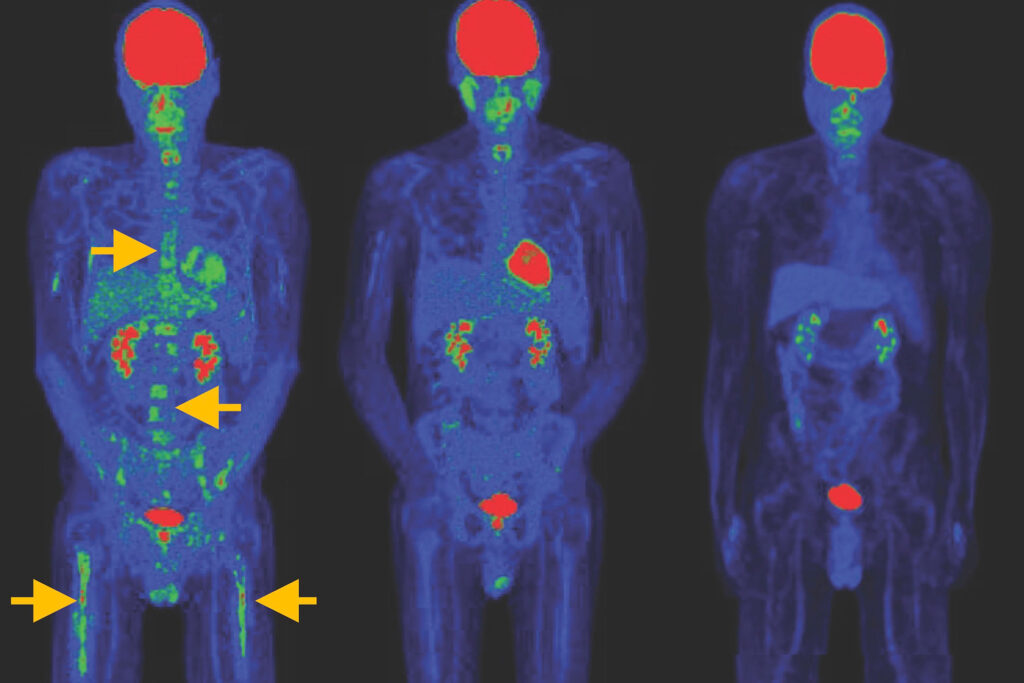
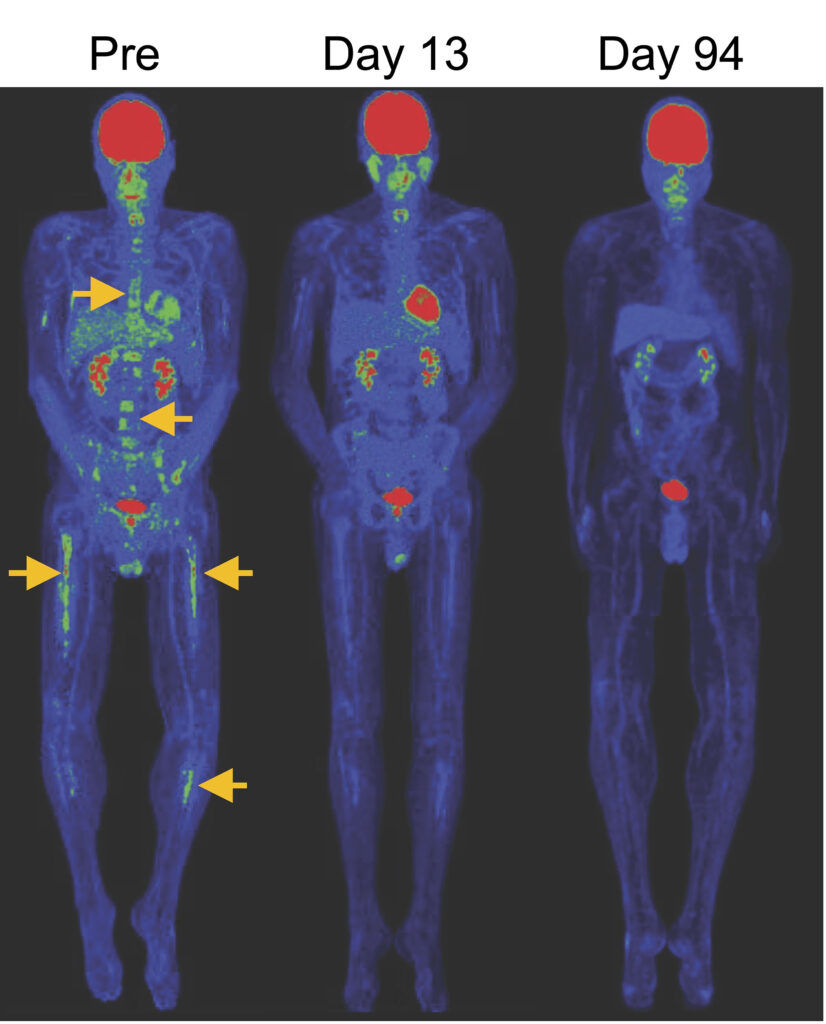
Die Bilder zeigen, wie sich Tumore nach der Behandlung mit speziellen CAR-T-Zellen deutlich zurückbildeten – und das sogar ohne vorbereitende Chemotherapie. © NIH
Bei Blutkrebs ist der Weg durch die Therapie oft lang und belastend. Vor einer CAR-T-Zelltherapie erhalten viele Patienten zunächst eine vorbereitende Chemotherapie, damit sich die neuen Immunzellen im Körper besser ausbreiten können. Diese Phase kostet Kraft und bringt oft zusätzliche Nebenwirkungen mit sich.
Nun berichten Forscher von einem anderen Ansatz. In einer frühen klinischen Studie konnten spezielle stammzellähnliche Immunzellen Tumore schon in sehr kleiner Menge vollständig zurückdrängen – ganz ohne diese vorbereitende Chemotherapie. Veröffentlicht wurde die Arbeit im Fachjournal Cell. Beteiligt war auch das Leibniz-Institut für Immuntherapie in Regensburg unter Leitung von Prof. Luca Gattinoni gemeinsam mit Dr. James Kochenderfer vom National Cancer Institute in den USA.
CAR-T-Zelltherapie scheitert oft an den eigenen Zellen
Bei der CAR-T-Zelltherapie werden körpereigene oder Spender-Immunzellen so verändert, dass sie Krebszellen gezielt erkennen und angreifen. Vor allem bei bestimmten Leukämien und Lymphomen hat das vielen Patienten neue Chancen eröffnet.
Das Problem liegt oft nicht nur am Tumor. Häufig verlieren die eingesetzten T-Zellen zu schnell ihre Kraft. Sie vermehren sich nicht stark genug oder verschwinden nach kurzer Zeit wieder aus dem Körper. Dann lässt die Wirkung nach.
Die neue Studie prüfte deshalb, ob die Art der eingesetzten Immunzellen wichtiger sein könnte als ihre Menge. Dafür verwendeten die Forscher sogenannte T-Stammgedächtniszellen, kurz TSCM-Zellen. Diese Zellen gelten als besonders langlebig. Sie können sich selbst erneuern und über längere Zeit neue Abwehrzellen nachliefern.
Erstautor Gabriele Inchingolo erklärt: „Aktuelle CAR-T-Produkte können stark variieren, und diese Heterogenität zeigt sich dann in unterschiedlichen Therapieerfolgen und Toxizitäten. Deshalb haben wir ein standardisiertes CD8+ CAR-T-Zellprodukt mit genau definierten Eigenschaften entwickelt.“

Weniger Zellen, aber bessere Ergebnisse
Untersucht wurden Patienten mit bestimmten Formen von Blutkrebs. Ihre Krebszellen trugen das Merkmal CD19 auf der Oberfläche. Daran können die veränderten Immunzellen sie erkennen. Alle Patienten hatten zuvor eine allogene Stammzelltransplantation erhalten. Dabei stammen die Stammzellen von einem Spender. Trotzdem war die Krankheit zurückgekehrt oder hatte auf frühere Therapien nicht ausreichend angesprochen. Für diese Patientengruppe gibt es oft nur noch wenige Behandlungsoptionen. Auffällig war vor allem die eingesetzte Zellmenge:
- Standard-CAR-T-Zellen: im Median 290 Millionen Zellen
- CAR-TSCM-Zellen: im Median nur 66 Millionen Zellen
Trotz der deutlich niedrigeren Dosis war die Gesamtansprechrate sogar besser:
- CAR-TSCM-Zellen: 55 Prozent
- Standard-CAR-T-Zellen: 45 Prozent
Noch deutlicher wurde der Unterschied bei vergleichbar niedrigen Dosen unter 300 Millionen Zellen. Dort erreichten 5 von 11 Patienten mit CAR-TSCM-Zellen eine komplette Remission. In der Standardgruppe gelang das nur bei 1 von 10 Patienten. „Die Zellen aus der TSCM-Plattform führten im Blut der Patienten zu einem höheren CAR-T-Zellspiegel – und in vielen Studien war das ein starker Prädiktor für klinischen Erfolg“, erklärt Dr. Kochenderfer.
Keine Chemotherapie vor der Infusion nötig
Normalerweise erhalten Patienten vor einer CAR-T-Zelltherapie eine vorbereitende Chemotherapie. Ärzte sprechen von Lymphodepletion. Sie soll Platz für die neuen Immunzellen schaffen und ihre Wirkung verbessern. Diese Phase belastet den Körper oft stark. Vor allem Menschen, die bereits mehrere Krebstherapien hinter sich haben, leiden darunter besonders.
In dieser Phase-1-Studie wurde bewusst darauf verzichtet. Alle Infusionen erfolgten ohne diese Vorbehandlung. So konnten die Forscher direkt vergleichen, wie sich die verschiedenen Zellprodukte im Körper verhalten. „Dass Patienten bei Dosen von nur 250.000 Zellen pro Kilogramm komplette Tumorrückbildungen erreichen, ganz ohne chemotherapeutische Vorbehandlung, bestätigt jahrelange Vorarbeit und eröffnet neue Möglichkeiten im CAR-T-Zelldesign“, sagt Prof. Gattinoni.
Für viele Patienten wäre das ein entscheidender Fortschritt: weniger Vorbehandlung, weniger Belastung und trotzdem eine starke Wirkung.
Auch die Nebenwirkungen fielen deutlich milder aus
Ein weiteres Problem vieler CAR-T-Behandlungen ist das sogenannte Zytokinfreisetzungs-Syndrom, kurz CRS. Dabei reagiert das Immunsystem sehr stark auf die Therapie. Es kann zu hohem Fieber, Kreislaufproblemen und schweren Entzündungsreaktionen kommen. Hier schnitten die neuen Zellen besser ab. In der TSCM-Gruppe gab es keinen einzigen Fall von CRS Grad 4. Nur ein Patient entwickelte ein CRS Grad 3. In der Standardgruppe traten bei 28,6 Prozent schwere CRS-Fälle der Grade 3 bis 4 auf.
Kochenderfer berichtet: „In dieser Studie kam es zu weniger Zytokinfreisetzungs-Syndromen als in den meisten anderen CAR-Studien, an denen ich beteiligt war.“ Selbst bei Zellmengen, die in der Vergleichsgruppe schwere CRS-Fälle auslösten, traten bei TSCM-Patienten meist nur milde Nebenwirkungen auf.
Die Immunzellen arbeiten wie ein langfristiges Reservelager
Die Forscher beobachteten noch einen wichtigen Unterschied. Standard-CAR-T-Zellen erreichten ihren Höhepunkt meist schon in der ersten Woche. Danach nahm ihre Aktivität oft wieder ab. Die TSCM-Zellen arbeiteten anders. Sie expandierten langsamer, erreichten ihren Höhepunkt erst in der zweiten Woche und blieben länger erhalten. Im Blut fanden die Forscher deutlich höhere Werte:
- CAR-TSCM-Zellen: median 30,4 CAR-T-Zellen pro Mikroliter
- Standard-CAR-T-Zellen: median 6,7 CAR-T-Zellen pro Mikroliter
Das bedeutet: Die Therapie wirkt nicht nur wie ein kurzer Angriff, sondern eher wie ein dauerhaftes Immunreservoir. Verschiedene Zellklone werden nach und nach aktiv. So bleibt ein Vorrat ruhender, stammzellähnlicher Zellen erhalten. „Die TSCM-Zellen werden nicht alle gleichzeitig aktiviert, sondern in kleinen aufeinanderfolgenden Wellen. Nacheinander werden unterschiedliche Klone aktiv, sodass das Gesamtreservoir erhalten bleibt“, erklärt Mitautor Dr. Enrico Lugli.
Noch ist es keine Standardtherapie
Die Studie liefert starke Hinweise, aber noch keine endgültige Antwort. Es handelt sich um eine frühe Phase-1-Studie mit 11 Patienten in der TSCM-Gruppe und 20 Patienten in der Vergleichsgruppe. Die Untersuchung war zudem nicht randomisiert. Wie bei Frühphasenstudien üblich, müssen größere randomisierte Studien folgen, um die Ergebnisse sicher zu bestätigen.
Die Forscher beobachteten außerdem, dass ein Therapieversagen oft nicht an den T-Zellen selbst lag. Gründe waren eher ein zu schwaches Zielprotein auf den Tumorzellen, hemmende Signale des Immunsystems wie Interleukin-10 oder Immunreaktionen gegen die CAR-Konstrukte selbst. Gattinoni fasst zusammen:
Wir haben gezeigt, dass ein klar definiertes, stammzellähnliches Zellprodukt bei niedrigeren Dosen wirksam sein kann.
Bei der CAR-T-Zelltherapie zählt also offenbar nicht nur die Menge der Zellen. Entscheidend kann sein, wie jung, langlebig und widerstandsfähig diese Immunzellen sind.
Kurz zusammengefasst:
- Bei der CAR-T-Zelltherapie ist nicht nur die Anzahl der Zellen wichtig, sondern vor allem ihre Qualität: stammzellähnliche T-Zellen (TSCM) bleiben länger aktiv, erneuern sich selbst und können Tumore dadurch wirksamer bekämpfen.
- In der Studie erreichten diese speziellen CAR-T-Zellen komplette Remissionen schon bei sehr niedrigen Dosen und sogar ohne vorbereitende Chemotherapie, was die Behandlung für viele Patienten deutlich schonender machen könnte.
- Auch schwere Nebenwirkungen wie das Zytokinfreisetzungs-Syndrom traten seltener auf, dennoch bleibt es bisher eine frühe Phase-1-Studie, deren Ergebnisse erst in größeren Studien bestätigt werden müssen.
Übrigens: Nicht nur neue Immuntherapien entscheiden über den Erfolg einer Krebsbehandlung – oft fällt die Entscheidung viel früher im Gewebe selbst. Forscher zeigen nun, wie winzige Tumoren bei Speiseröhrenkrebs sich ein schützendes Umfeld aufbauen, lange bevor Ärzte sie entdecken. Mehr dazu in unserem Artikel.
Bild: © NIH