Alzheimer-Todeskomplex entdeckt: Neuer Wirkstoff könnte den geistigen Abbau stoppen
Forscher entdecken bei Alzheimer einen tödlichen Proteinkomplex. Ein neuer Hemmstoff schützt Nervenzellen und bremst den kognitiven Abbau.
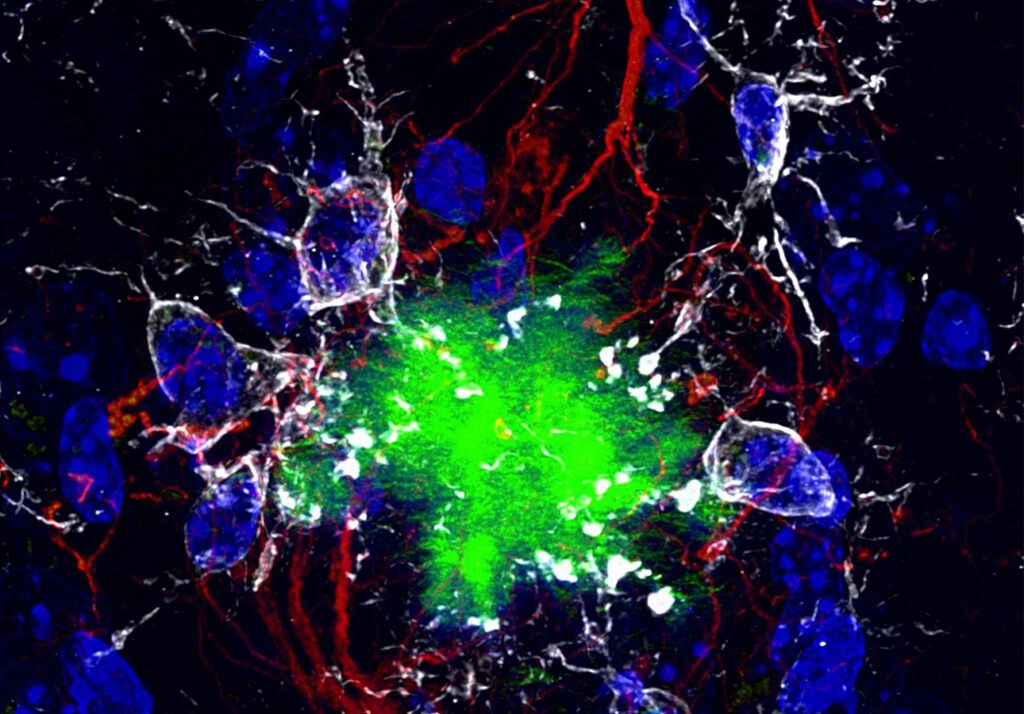
Tödliche Allianz im Gehirn: Der Alzheimer-Todeskomplex aus zwei Proteinen bringt Nervenzellen aus dem Gleichgewicht und beschleunigt die Krankheit. © Wikimedia
Vergessene Namen, verlegte Gegenstände, Orientierungslosigkeit: Alzheimer gilt als die Schreckensdiagnose des Alterns. In Deutschland leben mehr als 1,8 Millionen Menschen mit der Erkrankung, jedes Jahr kommen rund 440.000 neue Fälle hinzu. Medikamente lindern bisher nur Symptome – den Niedergang der Nervenzellen im Gehirn können sie nicht aufhalten. Nun aber liefert ein Forschungsteam der Uni Heidelberg einen Befund, der das Verständnis der Krankheit verändern könnte: Im Zentrum steht ein Eiweißkomplex, den die Wissenschaftler „Todeskomplex“ nennen.
Alzheimer – Wie der Todeskomplex Nervenzellen zerstört
Im gesunden Gehirn sichern sogenannte NMDA-Rezeptoren die Kommunikation zwischen Nervenzellen. Sie helfen beim Lernen und Speichern von Erinnerungen. Doch sobald sich diese Rezeptoren mit einem weiteren Protein, dem Ionenkanal TRPM4, verbinden, kippt ihre Funktion ins Gegenteil. Gemeinsam entwickeln sie toxische Eigenschaften, die Zellen schädigen und absterben lassen.
Dieser Mechanismus tritt bei Alzheimer-Patienten gehäuft auf. „Der NMDAR/TRPM4-Todeskomplex ist ein wesentlicher Treiber des Fortschreitens von Alzheimer“, schreiben die Forscher in der Fachzeitschrift Molecular Psychiatry. Mit anderen Worten: Der Komplex ist ein zentraler Motor des geistigen Abbaus.
Ein neues Molekül blockiert den Krankmacher
Die Forscher entwickelten ein kleines Molekül mit der Bezeichnung FP802. Es bindet an die Kontaktstelle zwischen NMDA-Rezeptor und TRPM4 und löst so den tödlichen Komplex auf. Damit bricht die Kette der Nervenschädigung zusammen.
Für ihre Versuche nutzten die Wissenschaftler das sogenannte 5xFAD-Mausmodell, das den Verlauf der Krankheit beim Menschen gut imitiert. Über vier Monate erhielten die Tiere FP802 oral verabreicht – in Dosierungen von 10 und 40 Milligramm pro Kilogramm Körpergewicht pro Tag.
Mäuse behalten ihr Gedächtnis
Die Resultate überraschten selbst die Forscher. Mäuse, die das Molekül bekamen, zeigten in Tests wie dem Morris-Wasserlabyrinth, einem Schwimmbecken mit versteckter Plattform zur Prüfung des räumlichen Gedächtnisses, deutlich bessere Leistungen. „Die Behandlung mit FP802 verhinderte den kognitiven Abbau bei Alzheimer-Mäusen“, heißt es im Bericht.
Auf mikroskopischer Ebene bestätigte sich der Befund: Nervenzellen blieben intakt. „Die Gabe von FP802 milderte den Verlust der dendritischen Komplexität und der Synapsendichte“, so die Autoren.
Schutz bis in die Zellkraftwerke
Ein weiterer Befund betrifft die Mitochondrien, die Kraftwerke der Zellen. Sie bleiben bei Alzheimer oft beschädigt, was die Energieversorgung des Gehirns zusätzlich schwächt. Mit FP802 blieben sie erstaunlich stabil. „FP802 schützt die Mitochondrien und erhält ihre strukturelle Integrität“, schreiben die Forscher.
Darüber hinaus waren die typischen Beta-Amyloid-Plaques im Gehirn der behandelten Tiere um 25 bis 40 Prozent geringer als bei der Kontrollgruppe. „FP802 verringert die Ablagerung von Amyloid-Plaques“, lautet ein weiteres Ergebnis.
Nebenwirkungen traten nicht auf
Die Wissenschaftler prüften die Organe der Mäuse sorgfältig. Weder Leber noch Niere oder Herz zeigten Anzeichen einer Schädigung. Das macht FP802 zu einem vielversprechenden Kandidaten für eine spätere klinische Anwendung.
Die Daten stammen aus Gruppen von sechs bis 15 Tieren pro Versuch und waren statistisch signifikant. Damit gilt der Befund als zuverlässig.
Auf einen Blick: Die wichtigsten Ergebnisse
- FP802 löst den Alzheimer-Todeskomplex aus NMDA-Rezeptor und TRPM4 auf
- Mäuse zeigten bessere Gedächtnisleistungen und Lernfähigkeit
- Nervenzellen behielten Struktur und Synapsendichte
- Mitochondrien blieben geschützt und funktionstüchtig
- Amyloid-Plaques reduzierten sich um 25–40 Prozent
- Keine Nebenwirkungen auf Leber, Niere oder Herz
Hoffnung auf neuen Therapieansatz
Die meisten bisherigen Medikamente richten sich gegen die Entstehung oder Entfernung von Amyloid-Plaques. Der neue Ansatz unterscheidet sich deutlich. Er blockiert einen Mechanismus, der nicht nur Nervenzellen zerstört, sondern auch die Bildung von Ablagerungen antreibt. „Unsere Entdeckung stellt einen bedeutenden Fortschritt auf diesem Gebiet dar“, so die Wissenschaftler.
Damit kann Alzheimer an einer zentralen biologischen Ursache angegangen werden – und nicht nur die Behandlung nur der Symptome oder Spätfolgen.
Neuer Wirkstoff schützt Nervenzellen nicht nur bei Alzheimer
Interessanterweise taucht derselbe Todeskomplex auch bei anderen Krankheiten auf, etwa bei der Amyotrophen Lateralsklerose (ALS). Erste Experimente deuten darauf hin, dass FP802 dort ebenfalls wirkt.
Sollte sich das bestätigen, könnte ein Wirkstofftyp mehrere neurodegenerative Erkrankungen beeinflussen – ein seltener und wertvoller Ansatz in der Medizin.
Noch viele Schritte bis zur Anwendung
Trotz der positiven Resultate bleibt die Therapie beim Menschen Zukunftsmusik. Vor einer klinischen Anwendung müssen Forscher das Molekül optimieren, umfassend auf Sicherheit prüfen und in mehreren Studienphasen testen.
„Die bisherigen Ergebnisse sind vielversprechend im präklinischen Kontext; bis zu einer möglichen Anwendung beim Menschen sind jedoch umfangreiche pharmakologische Entwicklungsarbeiten, toxikologische Untersuchungen sowie klinische Studien erforderlich“, erklärt Forschungsleiter Hilmar Bading.
Kurz zusammengefasst:
- Alzheimer wird durch einen schädlichen Proteinkomplex aus NMDA-Rezeptor und TRPM4 beschleunigt, der Nervenzellen zerstört.
- Das Molekül FP802 kann diesen Alzheimer-Todeskomplex auflösen, Nervenzellen schützen und den kognitiven Abbau in Tierversuchen deutlich verlangsamen.
- Erste Ergebnisse sind vielversprechend, doch bis zur Anwendung beim Menschen sind umfangreiche Prüfungen und klinische Studien notwendig.
Übrigens: Neben dem neu entdeckten Todeskomplex rückt nun auch ein Mangel an Lithium in den Fokus der Forschung: Wissenschaftler der Harvard University fanden stark verringerte Lithiumwerte im Gehirn von Alzheimer-Patienten – ein möglicher Frühfaktor für den Krankheitsprozess. Mehr dazu in unserem Artikel.
Bild: © Nicocapelo via Wikimedia unter CC BY-SA 4.0