Neues Eisen-Nanomaterial zerstört Krebszellen – gesundes Gewebe bleibt verschont
Ein neu entwickeltes Eisen-Nanomaterial zerstört Krebszellen gezielt. In Mäusen verschwand Brustkrebs ohne Schäden an gesundem Gewebe.
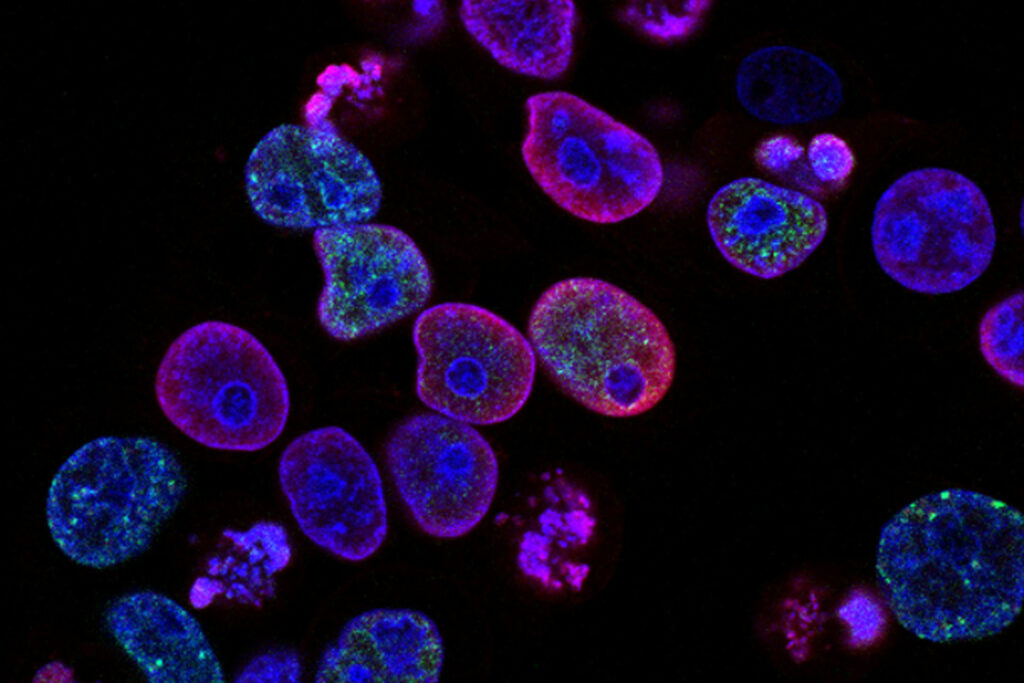
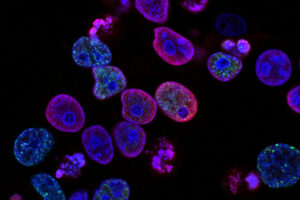
Forschende der Oregon State University entwickelten ein neues Eisen-Nanomaterial, das Krebszellen gezielt angreift und sie von innen heraus zerstört. (Symbolbild) © Unsplash
Krebsmedikamente wirken oft mit voller Wucht. Sie töten Tumorzellen, schädigen aber auch gesunde Zellen im Körper. Viele Patientinnen und Patienten kämpfen deshalb mit massiven Nebenwirkungen. Die Medizin sucht seit Jahren nach Therapien, die gezielter arbeiten. Ein neu entwickeltes Eisen-Nanomaterial soll Krebs nun direkt im Tumor angreifen und gesundes Gewebe verschonen. Im Mausmodell verschwand Brustkrebs damit vollständig.
Die Ergebnisse wurden in der Fachzeitschrift Advanced Functional Materials veröffentlicht. Beteiligt war ein Team der Oregon State University. Das Material nutzt eine typische Schwäche von Tumoren: ihre veränderte chemische Umgebung.
Tumorzellen besitzen ein anderes chemisches Milieu
Krebszellen unterscheiden sich deutlich von gesundem Gewebe. Sie sind saurer. Zudem enthalten sie höhere Konzentrationen von Wasserstoffperoxid. Diese Substanz kennt man als Desinfektionsmittel. In Tumoren entsteht sie jedoch natürlicherweise in größeren Mengen.
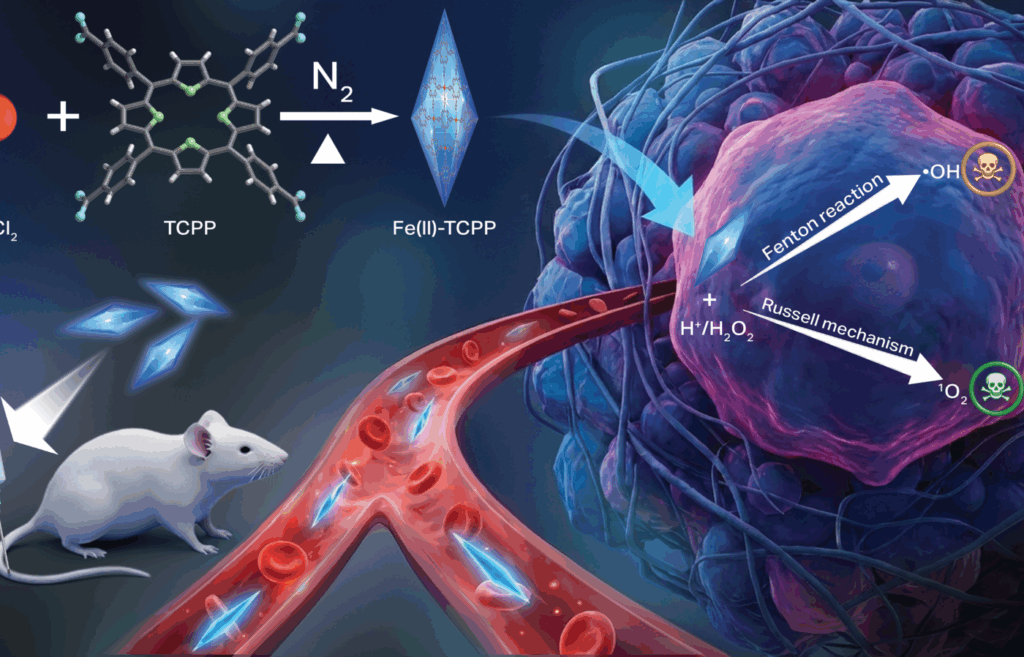
Diese Umgebung macht sich die neue Nanotherapie zunutze. Das Material besteht aus einem sogenannten Metall-organischen Gerüst. Dabei ist zweiwertiges Eisen in eine porphyrinhaltige Struktur eingebaut. Die Form ähnelt winzigen Nadeln. Dadurch entsteht eine große aktive Oberfläche.
Zwei Reaktionen greifen Krebszellen gleichzeitig an
Sobald das Material in eine Krebszelle gelangt, starten zwei chemische Prozesse gleichzeitig:
- Es entstehen Hydroxylradikale.
- Es bildet sich Singulett-Sauerstoff.
Beide gehören zu den reaktiven Sauerstoffspezies. Diese Moleküle sind extrem reaktionsfreudig. Sie entziehen wichtigen Zellbestandteilen Elektronen. Lipide, Proteine und sogar die DNA werden geschädigt. Die Krebszelle gerät unter massiven oxidativen Stress und stirbt ab.
Gesunde Zellen enthalten deutlich weniger Wasserstoffperoxid. Deshalb läuft diese doppelte Reaktion dort kaum ab. Das erklärt die beobachtete Selektivität.
Bisherige Ansätze reichten oft nicht aus
Das Verfahren gehört zur sogenannten chemodynamischen Therapie, kurz CDT. Dieser Ansatz nutzt die chemischen Besonderheiten von Tumoren. Bisher konnten CDT-Wirkstoffe meist nur eine Art reaktiver Sauerstoffverbindung erzeugen. „Bestehende CDT-Wirkstoffe sind begrenzt. Sie erzeugen entweder Hydroxylradikale oder Singulett-Sauerstoff, aber nicht beides“, erklärt Studienleiter Oleh Taratula. Außerdem fehle häufig die nötige katalytische Aktivität. Deshalb sei in präklinischen Studien oft nur eine teilweise Tumorverkleinerung erreicht worden. Ein dauerhafter Effekt blieb aus.
Das neue Eisen-Nanomaterial kombiniert erstmals beide Mechanismen in einer Struktur. Gleichzeitig weist es laut Studie eine höhere katalytische Effizienz auf. In Zellversuchen zeigte sich eine starke Wirkung gegen mehrere Krebszelllinien. Nicht-malignes Gewebe blieb weitgehend unbeschädigt.
Im Mausmodell verschwand Brustkrebs vollständig
Besonders deutlich wurden die Ergebnisse im Tierversuch. Mäuse mit menschlichen Brustkrebszellen erhielten den Wirkstoff über den Blutkreislauf. „Als wir unseren Nano-Wirkstoff Mäusen mit menschlichen Brustkrebszellen verabreichten, sammelte er sich effizient im Tumor an und beseitigte den Krebs vollständig, ohne Nebenwirkungen“, so Taratula. „Wir beobachteten eine vollständige Tumorregression und eine langfristige Verhinderung eines Rückfalls, ohne systemische Toxizität.“
Das heißt: Die Tumoren bildeten sich vollständig zurück. Während des Beobachtungszeitraums kehrten sie nicht zurück. Hinweise auf Organschäden oder andere systemische Nebenwirkungen fanden die Forschenden nicht.
Noch keine Therapie für Patienten
Trotz der vielversprechenden Ergebnisse handelt es sich um präklinische Daten. Bevor eine Anwendung beim Menschen möglich wird, sind weitere Untersuchungen nötig. Das Team plant Tests bei anderen Krebsarten, darunter aggressiver Bauchspeicheldrüsenkrebs. Erst danach könnten klinische Studien folgen. Ob sich die Ergebnisse aus dem Mausmodell auf den Menschen übertragen lassen, bleibt bis dato offen.
Finanziert wurde die Arbeit unter anderem vom National Cancer Institute der USA sowie vom Eunice Kennedy Shriver National Institute of Child Health and Human Development.
Kurz zusammengefasst:
- Das neu entwickelte Eisen-Nanomaterial greift Krebs gezielt an, indem es in Tumorzellen zwei aggressive Sauerstoffreaktionen auslöst und gesundes Gewebe weitgehend schont.
- In Mäusen mit menschlichen Brustkrebszellen führte die Behandlung zu einer vollständigen Tumor-Rückbildung ohne erkennbare Nebenwirkungen oder Rückfälle.
- Vor einer Anwendung beim Menschen sind weitere Untersuchungen bei unterschiedlichen Krebsarten notwendig, doch der Ansatz eröffnet Perspektiven für präzisere und möglicherweise nebenwirkungsärmere Therapien.
Übrigens: Eine große US-Analyse mit rund 26.000 Erwachsenen zeigt, dass Menschen mit höherer Kreatinaufnahme seltener an Krebs erkrankt waren. Warum Alter trotzdem der entscheidende Risikofaktor bleibt und was das für die Ernährung bedeutet, mehr dazu in unserem Artikel.
Bild: © Unsplash