Neu entdeckter Zellmechanismus spielt womöglich auch bei Demenz und Krebs eine Rolle
Eine neue Studie erklärt, wie gestörte Lysosomen den Zellstress erhöhen. Das könnte helfen, Demenz und Krebs besser zu verstehen.
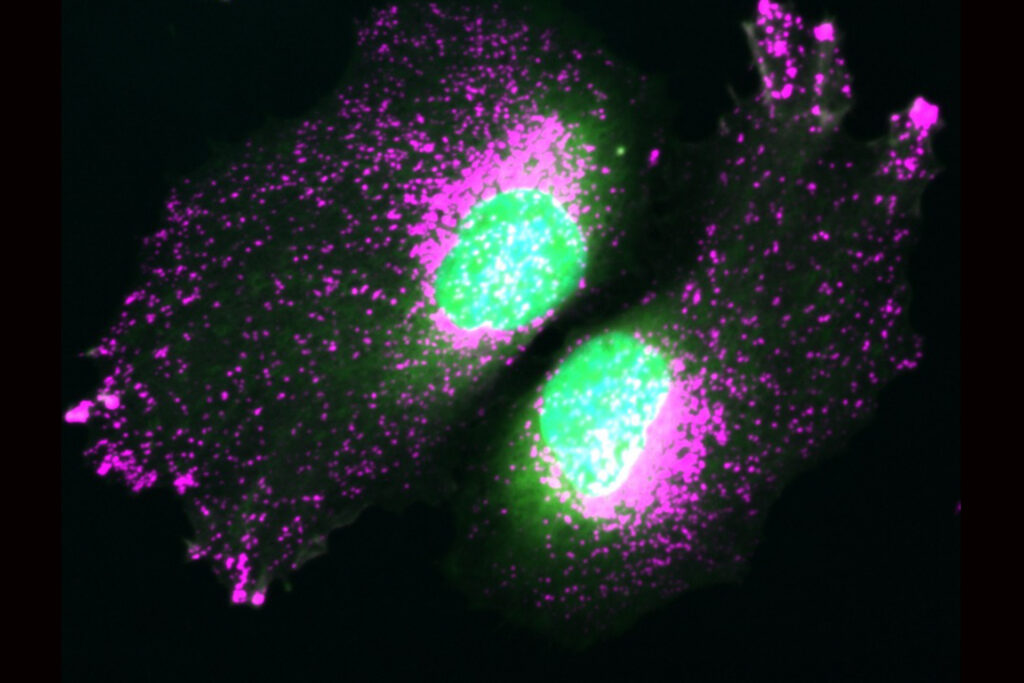
Das Mikroskopbild zeigt Zellen ohne das Protein TBC1D9B. Dadurch geraten die Lysosomen aus ihrer Ordnung, was den Zellstress erhöhen kann. © Klaudia Kosieradzka, FMP, Berlin
Wenn Zellen ihren eigenen Abfall nicht mehr sauber entsorgen, kann das ernste Folgen haben. Dieser Prozess spielt bei Krankheiten wie Alzheimer, Parkinson oder Krebs eine wichtige Rolle. Forscher haben nun einen Mechanismus entschlüsselt, der erklärt, warum das Recycling in der Zelle aus dem Takt geraten kann. Dabei geht es um winzige Zellbestandteile, die Eiweißreste abbauen und auf Nährstoffmangel reagieren. Gerät ihre Steuerung durcheinander, steigt der Zellstress. Dann verliert die Zelle einen Teil ihrer inneren Ordnung.
Veröffentlicht wurde die Arbeit in Nature Communications. Beteiligt waren Forscher der Universität Bielefeld, des Leibniz-Forschungsinstituts für Molekulare Pharmakologie in Berlin und der Christian-Albrechts-Universität zu Kiel. Im Kern geht es um Lysosomen. Diese kleinen Bläschen zerlegen alte oder defekte Eiweiße. Zugleich helfen sie der Zelle bei der Entscheidung, ob sie wachsen oder Energie sparen soll. Die Arbeit zeigt, dass Lysosomen nicht nur richtig arbeiten müssen, sie müssen auch am richtigen Ort in der Zelle sitzen.
Neuer Schalter bremst Zellstress
Lysosomen sind die Müllabfuhr und Recyclingstation der Zelle. Sie bleiben aber nicht einfach an einem festen Ort. Sie wandern dorthin, wo sie gebraucht werden. Das ist wichtig, weil ihre Aufgabe je nach Position etwas anders ausfällt. Fehlen der Zelle Nährstoffe, rücken sie normalerweise näher an die Mitte. Dort kann die Zelle ihre Selbstreinigung besonders wirksam anschalten. Bleibt diese Bewegung aus, gerät der Abbau ins Stocken.
Die Forscher haben in ihrer Arbeit einen fehlenden Teil in diesem Steuersystem gefunden. Vereinfacht gesagt geht es um eine Art Gas und Bremse. Das Eiweiß ARL8B treibt die Lysosomen eher an den Rand der Zelle. Dort unterstützen sie eher Vorgänge, die mit Wachstum zu tun haben. Lange blieb aber unklar, wer dieses Signal wieder stoppt und die Bewegung neu ordnet.
Diesen Gegenspieler haben die Teams nun identifiziert. Er heißt TBC1D9B. „Wir zeigen zum ersten Mal, welcher Gegenspieler den zentralen Transportschalter ARL8B wieder ausschaltet“, sagt Studienleiter Markus Damme von der Universität Bielefeld. TBC1D9B wirkt also wie eine Bremse. Es hilft dabei, ARL8B gezielt abzuschalten, damit die Lysosomen nicht dauerhaft am falschen Ort bleiben. Unterstützt wird es dabei von einem weiteren Eiweiß namens TMEM55B, das direkt an den Lysosomen sitzt.
Für die Zelle reicht nicht, dass ihre Recyclingstationen grundsätzlich arbeiten. Sie müssen auch rechtzeitig am richtigen Ort ankommen. Sitzen sie falsch, läuft die Reinigung schlechter. Dann bleiben eher schädliche Reste zurück. Solche Störungen gelten bei Krankheiten wie Alzheimer, Parkinson und Krebs als problematisch.
Zellstress bringt Lysosomen aus der Ordnung
In mehreren Versuchsreihen konnten die Teams diesen Effekt nachweisen. Sie schalteten TBC1D9B oder seinen Bindungspartner TMEM55B in Zellen aus. Danach verteilten sich Lysosomen ungeordnet bis an den Zellrand. Unter Nährstoffmangel kehrten sie nicht mehr wie üblich zum Zellzentrum zurück. Auch der Abbau lief schlechter. Die Autophagie litt ebenfalls. Das ist der Prozess, mit dem Zellen beschädigte Bestandteile zerlegen und wiederverwerten.
„Fehlt TBC1D9B oder sein Partner TMEM55B, verlieren Lysosomen ihre geordnete Position. Sie verteilen sich unkontrolliert in der Zelle“, sagt Studienautor Valentin Duhay von der Universität Kiel. Noch deutlicher wird die Störung bei Nährstoffmangel. Mitautorin Miaomiao Tian erklärt: „Normalerweise rücken Lysosomen dann ins Zellzentrum und kurbeln den Abbauprozess – die sogenannte Autophagie, eine Art Selbstreinigung der Zelle – an. Ohne den neu entdeckten Regulator funktioniert diese Anpassung nicht.“
Viele denken bei Zellbiologie zuerst an chemische Reaktionen. Hier geht es aber auch um räumliche Ordnung. Eine Zelle sortiert Belastung nicht nur über Botenstoffe. Sie verschiebt auch ihre Werkzeuge. Volker Haucke, der ebenfalls an der Studie beteiligt war, sagt dazu: „Damit verstehen wir besser, wie Zellen ihre Recyclingzentren – oder noch konkreter, ihre Nachhaltigkeitszentren – räumlich organisieren und an Nährstoffmangel anpassen.“
Der neue Mechanismus der Lysosomen könnte erklären, wie Krankheiten entstehen. Wenn ihre Kontroll- und Recyclingfunktion gestört ist, können sich schädliche Eiweißablagerungen im Gehirn ansammeln. Tumorzellen können dieselben Systeme dagegen für ihr eigenes Wachstum nutzen.
Neuer Angriffspunkt für Demenz- und Krebsforschung
Die Forscher nutzten für ihre Arbeit unter anderem Proteomanalysen, Genom-Editierung und hochauflösende Mikroskopie. Dadurch konnten sie den Ablauf sehr genau verfolgen. Entscheidend war dabei nicht nur, dass Lysosomen falsch sitzen. Die Studie zeigt auch eine Kette von Ursachen. Fehlt TBC1D9B, bleibt ARL8B zu aktiv. Dann geraten die Lysosomen an die falsche Stelle. Danach reagiert die Zelle schlechter auf Belastung.
Für Erkrankungen wie Alzheimer oder Parkinson ist das besonders interessant. Dort gilt seit Jahren als Problem, dass Eiweiße nicht mehr richtig entsorgt werden. Bei Krebs ist die Lage anders, aber ebenfalls heikel. Tumorzellen brauchen Rohstoffe und flexible Stoffwechselwege. Auch dafür spielen Lysosomen eine wichtige Rolle.
Die Arbeit beschreibt keine fertige Therapie. Sie zeigt keinen neuen Wirkstoff. Sie beweist auch nicht, dass Demenz oder Krebs bald verhindert werden können. Sie liefert aber einen präzisen Angriffspunkt für weitere Forschung. „Unsere Ergebnisse liefern den fehlenden Baustein zur Regulation von ARL8B. Diese Entdeckung eröffnet neue Perspektiven, um krankhafte Prozesse wie das Tumorwachstum gezielt zu beeinflussen“, so Damme.
Haucke blickt bereits etwas weiter nach vorn. Er sagt: „Durch gezielte Eingriffe in die Schaltprozesse am Lysosom könnten wir z.B. Nervenzellen widerstandsfähiger machen und so Demenz verhindern oder verzögern oder Immunzellen, die ebenfalls von ARL8 abhängig sind, scharfstellen, um Viren oder Bakterien effektiver zu bekämpfen.“
Kurz zusammengefasst:
- Lysosomen sind die Recyclingstationen der Zelle, und ihre genaue Position entscheidet mit darüber, ob Abfall abgebaut oder Zellstress ausgelöst wird.
- Das Protein TBC1D9B wirkt als wichtiger Gegenschalter für ARL8B; fehlt dieser Mechanismus, geraten Lysosomen an die falsche Stelle, und Selbstreinigung sowie Reaktion auf Nährstoffmangel funktionieren schlechter.
- Der Befund erklärt besser, warum ähnliche Störungen bei Demenz, Parkinson und Krebs eine Rolle spielen, auch wenn daraus noch keine fertige Therapie folgt.
Übrigens: Während ein neuer Zellmechanismus erklärt, wie gestörte Recyclingprozesse den Zellstress erhöhen, zeigt Alzheimer-Forschung nun, warum manche Nervenzellen selbst bei Tau-Ablagerungen länger standhalten. Entscheidend ist ihre innere Müllabfuhr, die schädliches Tau erkennt, abbaut und so den Zellbetrieb stabil hält. Mehr dazu in unserem Artikel.
Bild: © Klaudia Kosieradzka, FMP, Berlin